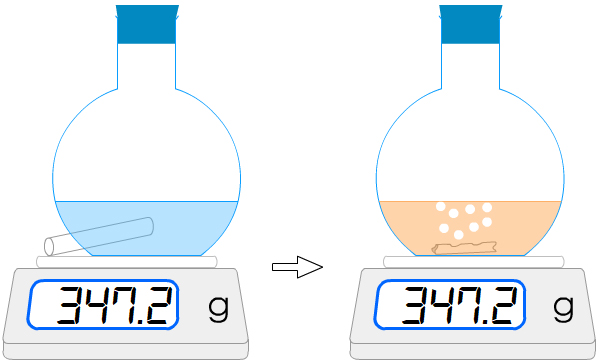
Bilan : Le carbone et le dioxygène disparaissent. Du dioxyde de carbone apparaît.

Bilan : Le méthane et le dioxygène disparaissent, le dioxyde de carbone et l’eau apparaissent.
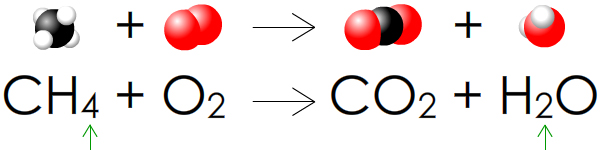
Problème : le nombre d’atomes d’hydrogène n’est pas le même avant et après ! Il faut EQUILIBRER.
La règle :
1. Surtout, ne pas toucher aux formules des molécules (le pb n’est pas là !)
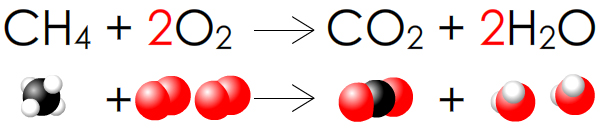
2. Placer le coefficient 2 devant H2O pour équilibrer H ;
3. Remarquer que ce geste a « déséquilibré » l’élément O ;
4. Placer le coefficient 2 devant O2 pour équilibrer O.
Expérience : On fait réagir de l’eau acidifiée sur du carbonate de calcium. On mesure la masse totale avant, pendant et après la transformation.