
‐ Expérience (vue en 5e) :
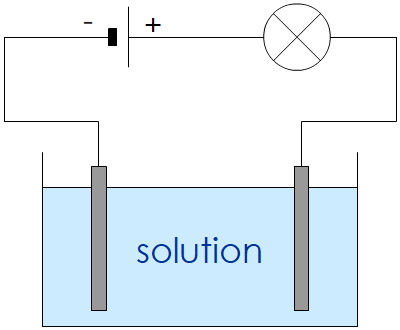
Observations :
‐ si la solution est de l’eau salée, l’ampoule brille ;
‐ si la solution est de l’eau sucrée, l’ampoule est éteinte.
Interprétation :
La lampe s’allume lorsqu’elle est parcourue par un courant électrique.Exemple de l’eau salée
C’est une solution de chlorure de sodium. Le soluté, le sel, est composé de cristaux de chlorure de sodium. Le solvant est l’eau. Dans la solution, il y a des ions chlorure et des ions sodium.
‐ L’ion sodium, de formule Na+, provient d’un atome de sodium qui a cédé un électron. Il est chargé positivement.
‐ L’ion chlorure, de formule Cl‐, provient d’un atome de chlore qui a gagné un électron. Il est chargé négativement.

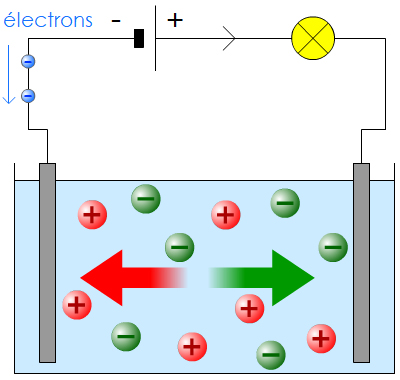
En rouge les ions positifs et en vert les ions négatifs.
Les molécules d’eau ne sont pas représentées ici.
Remarque 1 : Les solides ioniques (cristaux de sel) ne conduisent pas le courant car les ions ne peuvent pas s'y déplacer.
Remarque 2 : Les ions métalliques sont tous positifs. Cu2+, Zn2+, Al3+…
Remarque 3 : Il existe des ions polyatomiques : ion ammonium NH4+, ion permanganate MnO4‐, ion sulfate SO42‐…